Как работают литий-ионные аккумуляторы: принцип работы, история, аноды, катоды и будущее Li-ion

Литий-ионный аккумулятор (Li-ion) — это перезаряжаемый электрохимический элемент, в котором ионы лития перемещаются между анодом и катодом во время зарядки и разрядки. Благодаря высокой плотности энергии Li-ion аккумуляторы стали основой современной портативной электроники, электромобилей и систем накопления энергии, но их история начинается с неудачных экспериментов с металлическим литием и драматических отзывов батарей в 1991 году.
Истоки литиевых батарей: от металлического лития до эпохи Li-ion
Пионерская работа над литиевыми батареями началась ещё в 1912 году под руководством американского химика Гилберта Ньютона Льюиса (G. N. Lewis), но до реальных продуктов было далеко. Лишь в начале 1970-х годов появились первые коммерческие неперезаряжаемые (primary) литиевые элементы, использующие металлический литий в качестве анода. Попытки создать перезаряжаемые литиевые аккумуляторы в 1980-х годах закончились провалом: оказалось, что металлический литий как анод слишком нестабилен при циклах заряд–разряд.
Важно различать два класса систем:
- Металло-литиевые батареи — используют металлический литий как анод.
- Литий-ионные батареи — используют графит (или другой углеродный / интеркаляционный материал) как анод и различные активные материалы (оксиды металлов) в катоде.
Литий — самый лёгкий металл с максимально высоким электрохимическим потенциалом, поэтому теоретически обеспечивает наивысшую удельную энергию среди металлических анодных систем. Аккумуляторы с металлическим литием на аноде действительно демонстрировали чрезвычайно высокую плотность энергии, но одновременно выявили серьёзную проблему безопасности.
Дендриты, тепловой разгон и знаменитый отзыв 1991 года
В середине 1980-х годов исследователи обнаружили, что при циклической зарядке–разрядке на поверхности металлического лития образуются дендриты — тонкие металлические «иглы» и ответвления. Эти дендриты прорастают через поры сепаратора и могут достичь противоположного электрода, вызывая внутреннее короткое замыкание.
Когда это происходит, сопротивление элемента резко падает, ток возрастает, и температура ячейки быстро повышается, приближаясь к точке плавления лития. Такой тепловой разгон может закончиться тепловым взрывом и «выбросом пламени» — внезапным разрядом с выбросом горячих газов и огня. Ситуация стала настолько серьёзной, что в начале 1990-х большая партия перезаряжаемых металло-литиевых батарей, отправленных в Японию, была отозвана после инцидента, когда аккумулятор мобильного телефона выбросил горящие газы и вызвал ожоги лица пользователя.
Внутренняя нестабильность металлического лития, особенно при зарядке, заставила отрасль практически отказаться от металлического лития как анодного материала и перейти к концепции литий-ионных систем, где литий присутствует в виде ионов, а не «чистого» металла.
Коммерциализация литий-ионных аккумуляторов: Sony, Goodenough и патентные споры
В 1991 году Sony коммерциализировала первый литий-ионный аккумулятор и установила новый стандарт для портативной энергетики. Хотя энергоёмкость Li-ion была ниже, чем у теоретических литий-металлических систем, новая химия оказалась значительно безопаснее при соблюдении ограничений по напряжению и току.
Одной из ключевых фигур в развитии Li-ion стал Джон Б. Гуденаф (John B. Goodenough, 1922–2023), который в конце 1970-х годов в Оксфордском университете показал, что оксид лития-кобальта (LiCoO₂) может служить высоковольтным катодным материалом для перезаряжаемых литий-ионных батарей. На основе этой катодной химии японский химик Акира Ёсино в компании Asahi Kasei в 1980-х годах создал первую коммерчески пригодную литий-ионную батарею, адаптировав разработки Гуденафа для промышленного применения в Японии. В 1991 году Sony объявила о международном патенте на катод LiCoO₂, что вызвало многолетние судебные споры. В итоге Sony сохранила контроль над патентом, а Гуденаф не получил финансового вознаграждения, соответствующего масштабу влияния его идеи.
Позже, в знак признания фундаментального вклада в развитие литий-ионных технологий, Национальная инженерная академия США в 2014 году присудила Гуденафу и другим ключевым разработчикам премию Чарльза Старка Дрейпера. В 2015 году Израиль отметил его работу премией в размере 1 млн долларов, которую Гуденаф передал Техасскому институту материалов для дальнейших исследований в области материаловедения.
Почему литий-ионные аккумуляторы такие энергоёмкие
Главный фактор высокой удельной энергии Li-ion — высокое напряжение ячейки около 3,6 В. В сочетании с относительно высокой ёмкостью это обеспечивает значительную энергию на единицу массы и объёма. Дальнейшее совершенствование активных материалов катода и анода, а также электролитов потенциально позволяет ещё повысить плотность энергии.
Кривая разряда литий-ионного элемента имеет относительно плоский профиль в рабочем диапазоне напряжения примерно 3,7–2,8 В на ячейку. Это означает, что большая часть накопленной энергии доступна в достаточно узком диапазоне напряжения, что упрощает проектирование силовой электроники и повышает эффективность использования энергии.
Таблица 1. Сравнение основных химий литий-ионных аккумуляторов
| Химия | Полное название | Номинальное напряжение | Плотность энергии | Безопасность | Ресурс циклов | Основные преимущества | Основные недостатки | Типичные применения |
|---|---|---|---|---|---|---|---|---|
| LiCoO₂ (LCO) | Литий-кобальт-оксид | 3,6–3,7 В | Очень высокая | Средняя | 500–1000 | Высокая энергоёмкость | Низкая термостабильность, дорогой кобальт | Смартфоны, ноутбуки, фотоаппараты |
| NMC | Никель-марганец-кобальт | 3,6–3,7 В | Высокая | Средняя | 1000–2000 | Баланс ёмкости, мощности и ресурса | Сложное охлаждение при высоких нагрузках | Электромобили, системы хранения энергии |
| NCA | Никель-кобальт-алюминий | 3,6–3,7 В | Очень высокая | Средняя-низкая | 1000–1500 | Максимальная энергоёмкость | Повышенная чувствительность к перегреву | Электромобили Tesla, авиация |
| LFP | Литий-железо-фосфат | 3,2–3,3 В | Средняя | Очень высокая | 2000–7000 | Безопасность, долговечность, стабильность | Низкая плотность энергии | Солнечные станции, электробусы, UPS |
| LTO | Литий-титанат | 2,3–2,4 В | Низкая | Чрезвычайно высокая | 10000–25000 | Экстремальный ресурс и быстрая зарядка | Высокая цена и низкая энергоёмкость | Промышленность, транспорт, военные системы |
Эволюция формата 18650: от 1100 до 3000+ мА·ч
Цилиндрический формат 18650 (диаметр 18 мм, длина 65 мм) стал одним из важнейших «строительных блоков» литий-ионной энергетики.
- В 1994 году себестоимость одного Li-ion 18650 превышала 10 долларов США, а ёмкость составляла около 1100 мА·ч.
- К 2001 году цена упала ниже 3 долларов США, а ёмкость выросла до ≈1900 мА·ч.
- Сегодня высокоэнергетические 18650 превышают 3000 мА·ч, а стоимость продолжает снижаться благодаря массовому производству и оптимизации материалов.
Снижение стоимости, увеличение удельной энергии и отсутствие высокотоксичных компонентов сделали литий-ионные аккумуляторы универсальным решением для портативной электроники, промышленных систем, электротранспорта и даже спутников.
Таблица 2. Эволюция формата 18650
| Год | Типичная ёмкость | Ориентировочная цена | Ключевые особенности |
|---|---|---|---|
| 1994 | ≈1100 мА·ч | >10 USD | Начало массового развития Li-ion |
| 2001 | ≈1900 мА·ч | <3 USD | Сильное удешевление производства |
| 2010 | 2400–2800 мА·ч | ≈2–4 USD | Широкое использование в ноутбуках и EV |
| 2025+ | 3000–4000+ мА·ч | Продолжает снижаться | Кремниевые добавки и оптимизация материалов |
Преимущества литий‑ионных аккумуляторов: почему они стали стандартом
Литий‑ионные батареи практически не требуют обслуживания, что резко отличает их от никелевых и свинцово‑кислотных систем. Они не обладают выраженным эффектом памяти и не требуют специальных «разрядных тренировок» для поддержания ёмкости. Уровень саморазряда — меньше половины, чем у NiCd и NiMH, что делает показатели уровня заряда (индикаторы SoC) значительно более надёжными.
Номинальное напряжение одного элемента (≈3,6 В) позволяет напрямую питать мобильные телефоны, планшеты, цифровые фотоаппараты и другие устройства без необходимости сложных многоклеточных конфигураций. Это упрощает шасси, уменьшает массу, снижает стоимость и повышает общую эффективность.
Основные преимущества Li‑ion:
- Высокая удельная энергия (Вт·ч/кг) и возможность реализации элементов с высокой удельной мощностью (power cells).
- Относительно длительный циклический ресурс и длительный календарный срок службы.
- Высокая ёмкость, низкое внутреннее сопротивление, высокий кулоновский КПД.
- Простой алгоритм зарядки (постоянный ток → постоянное напряжение) и относительно короткое время зарядки.
- Низкий саморазряд (меньше половины NiCd/NiMH).
Ограничения:
- Необходимость защитных схем (BMS) для предотвращения перенапряжения, глубокого разряда и перегрева, что может привести к тепловому разгону.
- Деградация при высоких температурах и длительном хранении при высоком напряжении (близко к полному заряду).
- Нежелательно быстрая зарядка при температурах ниже 0°C (риск литиевого плакирования).
- Необходимость соблюдения транспортных правил при перевозке крупных партий Li‑ion.
Как работает литий‑ионный аккумулятор: анод, катод и движение ионов
Литий‑ионный элемент состоит из трёх ключевых компонентов:
- Катод (положительный электрод) — оксид металла (например, LiCoO₂, NMC, NCA и др.), нанесённый на алюминиевый токосъёмник.
- Анод (отрицательный электрод) — обычно графит или иной углеродный материал, нанесённый на медный токосъёмник.
- Электролит и сепаратор — органический жидкий электролит с солями лития и пористый сепаратор, который пропускает ионы, но блокирует электроны.
Во время разряда ионы лития движутся от анода к катоду через электролит, а электроны — через внешнюю цепь, совершая работу. При этом анод подвергается окислению (отдаёт электроны), катод — восстановлению (принимает электроны). Во время зарядки процесс идёт в обратном направлении: ионы лития «закачиваются» назад в анод, а электроны возвращаются через зарядную цепь.
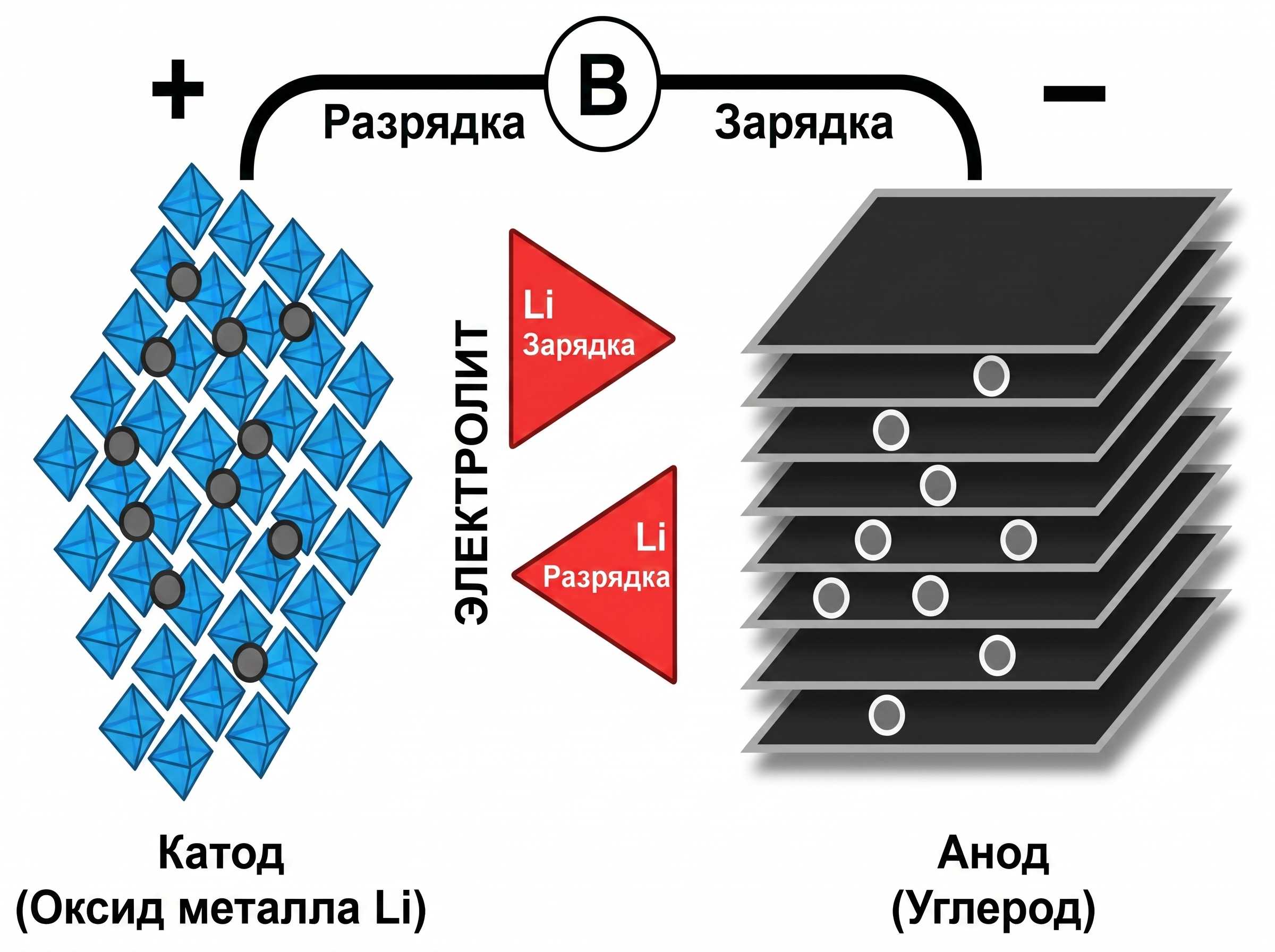
Рисунок 1: Поток ионов в литий‑ионном аккумуляторе.
Во время зарядки и разрядки элемента ионы перемещаются между катодом (положительный электрод) и анодом (отрицательный электрод). Во время разряда анод подвергается окислению или потере электронов, а катод — восстановлению или приёму электронов. При зарядке процесс происходит в обратную сторону.
От кокса до графита и дальше: эволюция анодных материалов
Первые литий‑ионные элементы Sony использовали кокс (побочный продукт нефтехимии) как анодный материал. В 1997 году большинство производителей, включая Sony, перешли на графит, чтобы получить более плоскую кривую разряда и лучшую циклическую стабильность. Графит — это распространённая форма углерода (знакомая нам, в частности, по грифелям карандашей), которая хорошо интеркалирует ионы лития и обладает длительным сроком службы.
Среди углеродных материалов для анода различают:
- графит (доминирующий на рынке)
- твердый и мягкий углерод
- нанотрубчатые формы (пока без широкого коммерческого использования из‑за склонности к агрегации).
В перспективе важную роль могут сыграть графен и композиты на его основе, которые обещают повышенную проводимость и потенциально лучшие механические свойства анода.
На кривых типа «кривые разряда» хорошо видно, что современный графитовый анод формирует значительно более плоский профиль напряжения, чем ранние коксовые варианты, что улучшает стабильность питания нагрузки.
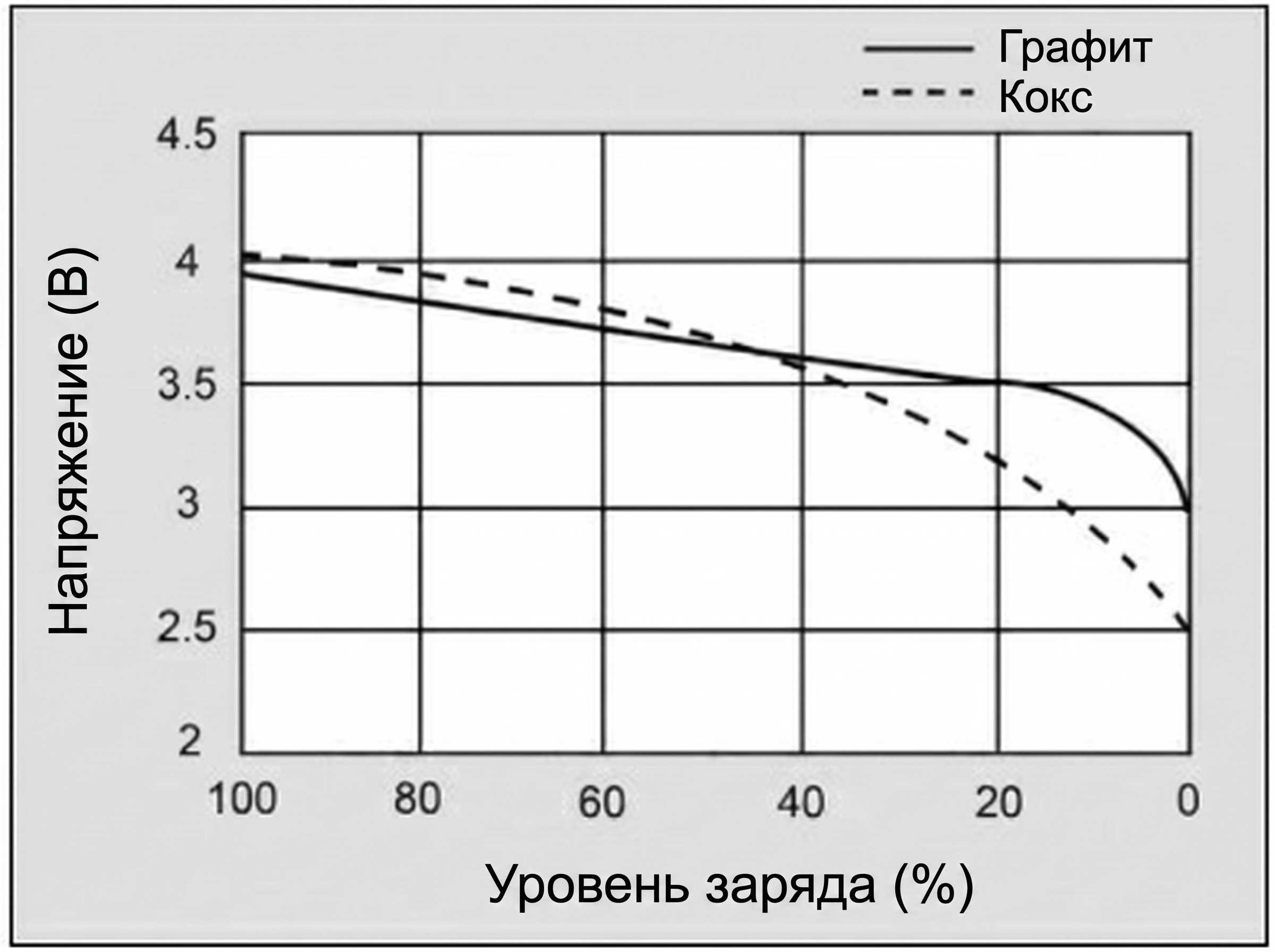
Рисунок 2: Кривая разряда литий‑ионного аккумулятора.
Аккумулятор должен иметь более плоскую кривую напряжения в рабочем диапазоне разряда. Современный графитовый анод делает это лучше, чем ранний коксовый вариант. Предоставлено компанией Cadex.
Кремниевые и титановые аноды: 10× потенциал и проблемы расширения
Чтобы повысить энергоёмкость Li‑ion, производители экспериментируют с добавлением кремния в анод. На атомарном уровне соотношение углерод : литий составляет приблизительно 6:1 — шесть атомов углерода могут связать один ион лития. Кремний же способен связывать до четырёх ионов лития на один атом, что теоретически открывает возможность увеличить ёмкость анода в ≈10 раз по сравнению с чистым графитом.
Главная проблема — объёмное расширение: при зарядке кремниевый анод может увеличиваться в объёме до 300%, что приводит к механическим разрушениям, трещинам и быстрой деградации. Поэтому чисто кремниевые аноды на текущем этапе непрактичны; вместо этого производители добавляют небольшое количество кремния (3–5%) в графитовую матрицу, повышая ёмкость без катастрофической потери ресурса.
Иной интересный путь — использование наноструктурированного литий‑титаната (LTO) в качестве анодного материала. LTO обеспечивает:
- очень длительный циклический ресурс (десятки тысяч циклов)
- высокие токоотводящие возможности
- отличные низкотемпературные характеристики
- повышенную безопасность и термостабильность, но за счёт меньшей удельной энергии и более высокой стоимости.
Таблица 3. Сравнение анодных материалов в Li‑ion аккумуляторах
| Материал анода | Удельная ёмкость | Преимущества | Недостатки | Статус использования |
|---|---|---|---|---|
| Графит | ≈372 мА·ч/г | Стабильность, низкая цена, длительный ресурс | Ограниченная ёмкость | Доминирует на рынке |
| Кремний | До ≈4200 мА·ч/г | Очень высокая теоретическая ёмкость | Расширение до 300%, деградация | Используется в композитах |
| LTO | ≈175 мА·ч/г | Безопасность, ресурс, быстрая зарядка | Низкая энергоёмкость | Специализированные системы |
| Твёрдый углерод | Средняя | Стабильность и низкая стоимость | Ниже проводимость | Частично используется |
| Графеновые композиты | Потенциально очень высокая | Высокая проводимость и механическая прочность | Высокая цена и сложное производство | Экспериментальные технологии |
«Энергетические», «силовые» и гибридные элементы Li‑ion
Модифицируя материалы анода и катода, производители могут настраивать элементы под разные задачи:
- Энергетический элемент (energy cell) — максимизирует удельную энергию, обеспечивая длительное время работы, но имеет более низкую удельную мощность.
- Силовой элемент (power cell) — оптимизирован под высокие токи и пиковые нагрузки, жертвуя частью ёмкости.
- Гибридный элемент (hybrid cell) — компромиссный вариант, предлагающий баланс между энергоёмкостью и мощностью.
Ещё одна ось настройки — соотношение кобальта и никеля в катоде:
- увеличение доли никеля снижает себестоимость и повышает ёмкость,
- но снижает термостабильность и безопасность.
Начинающие игроки стремятся быстро выйти на рынок, предлагая высокую энергоёмкость и низкие цены, но это часто происходит за счёт долговечности и безопасности. Добросовестные производители отдают приоритет именно безопасности, стабильности и предсказуемому старению.
Таблица 4. Сравнение типов Li‑ion элементов по назначению
| Тип элемента | Основной приоритет | Удельная энергия | Удельная мощность | Типичные применения |
|---|---|---|---|---|
| Energy Cell | Максимальная ёмкость | Очень высокая | Средняя | Ноутбуки, смартфоны, электромобили |
| Power Cell | Высокий ток | Средняя | Очень высокая | Электроинструмент, дроны, спорткары |
| Hybrid Cell | Баланс параметров | Высокая | Высокая | Универсальные батарейные системы |
Структура элемента Li‑ion и краткое резюме плюсов/минусов
Типичный литий‑ионный элемент имеет такую структуру:
- Катод: слой оксида металла на алюминиевом токосъёмнике.
- Анод: слой графита / углерода на медном токосъёмнике.
- Сепаратор: пористая полимерная плёнка, разделяющая электроды и пропускающая только ионы.
- Электролит: органический растворитель с литиевой солью, переносящий ионы между электродами.
Обобщённые преимущества Li‑ion:
- Высокая удельная энергия и возможность реализовать высокие нагрузки в «силовых» вариантах.
- Длительный циклический ресурс и длительный срок хранения.
- Низкое внутреннее сопротивление, высокий КПД, простой алгоритм зарядки.
- Низкий саморазряд и отсутствие выраженного эффекта памяти.
Обобщённые ограничения:
- Необходимость BMS и защитных схем для предотвращения теплового разгона.
- Чувствительность к высокой температуре и длительному нахождению при высоком напряжении (полном заряде).
- Ограничения на быструю зарядку при низких температурах.
- Транспортные требования при перевозке крупных партий аккумуляторов.
Литий‑ионные аккумуляторы, несмотря на свои ограничения, стали ключевой технологией энергетического перехода — от смартфонов и ноутбуков до электромобилей и систем накопления энергии, задавая вектор развития материаловедения, электрохимии и инженерии батарей на десятилетия вперёд.
Таблица 5. Сравнение Li‑ion, NiMH и свинцово‑кислотных аккумуляторов
| Параметр | Li‑ion | NiMH | Свинцово‑кислотный |
|---|---|---|---|
| Плотность энергии | Высокая | Средняя | Низкая |
| Саморазряд | Низкий | Высокий | Низкий |
| Эффект памяти | Практически отсутствует | Умеренный | Отсутствует |
| Масса | Низкая | Средняя | Высокая |
| Ресурс циклов | 500–3000+ | 300–700 | 200–500 |
| Обслуживание | Минимальное | Минимальное | Может требовать обслуживания |
| Типичные применения | Электроника, EV, ESS | Побутовая техника | UPS, авто‑стартеры |
Будущее литий‑ионных аккумуляторов: современные тренды и новые технологии
Несмотря на доминирование классических Li‑ion аккумуляторов, отрасль батарейных технологий переживает один из самых быстрых этапов развития в истории электрохимии. Производители электромобилей, портативной электроники и систем накопления энергии активно работают над повышением плотности энергии, скорости зарядки, ресурса и безопасности аккумуляторов.
Среди ключевых направлений развития — твёрдотельные батареи (solid‑state batteries), кремниевые аноды, натрий‑ионные системы, высоконикелевые катоды и новые производственные технологии, такие как dry‑electrode manufacturing.
Твёрдотельные аккумуляторы (Solid‑State Batteries)
Твёрдотельные аккумуляторы заменяют жидкий органический электролит твёрдым ионопроводящим материалом. Это потенциально позволяет:
- значительно повысить безопасность,
- снизить риск теплового разгона,
- использовать металлический литий в качестве анода,
- повысить плотность энергии на 30–70%.
Основными проблемами solid‑state остаются высокая стоимость, сложность производства и деградация контактов между твёрдыми материалами при циклах зарядки.
Кремниевые аноды нового поколения
Одним из самых активных направлений развития является постепенное увеличение доли кремния в анодах. Кремний имеет теоретическую ёмкость во много раз выше, чем графит, что позволяет:
- увеличить автономность электромобилей,
- уменьшить массу батарей,
- повысить скорость зарядки.
Современные производители уже используют графит‑кремниевые композиты, но высокий уровень объёмного расширения кремния по‑прежнему остаётся ключевой инженерной проблемой.
Натрий‑ионные аккумуляторы (Sodium‑Ion)
Натрий‑ионные батареи (Na‑ion) считаются перспективной альтернативой Li‑ion для стационарных систем накопления энергии и бюджетного транспорта.
Их основные преимущества:
- ниже стоимость сырья,
- меньшая зависимость от лития и кобальта,
- лучшая работа при низких температурах.
Недостатком натрий‑ионных систем пока остаётся более низкая плотность энергии по сравнению с классическими Li‑ion аккумуляторами.
Высоконикелевые катоды и снижение доли кобальта
Современные катодные материалы постепенно переходят к высоконикелевым композициям (NMC 811, NCA и др.), которые позволяют повысить энергоёмкость и снизить использование дорогого кобальта.
Однако увеличение доли никеля одновременно:
- повышает чувствительность к перегреву,
- усложняет термостабилизацию,
- повышает требования к системам охлаждения и BMS.
Технология dry‑electrode manufacturing
Одним из самых перспективных направлений производства батарей является dry‑electrode manufacturing — технология нанесения электродов без использования жидких растворителей.
Преимущества такого подхода:
- снижение энергопотребления производства,
- упрощение технологического процесса,
- снижение себестоимости батарей,
- меньшее экологическое воздействие.
Эта технология активно исследуется для будущих высокопроизводительных аккумуляторных платформ.
Формат 4680 и новое поколение цилиндрических элементов
Новые цилиндрические элементы формата 4680 (46 × 80 мм) создаются для увеличения энергоёмкости и снижения стоимости батарейных модулей.
По сравнению с 18650 и 21700 формат 4680 обеспечивает:
- более высокую энергетическую плотность,
- меньшее количество соединений в батарейном пакете,
- лучшее соотношение массы и ёмкости,
- снижение производственных затрат.
В то же время крупные элементы создают новые вызовы в области теплоотвода и контроля температуры.
Сравнение перспективных батарейных технологий
Таблица 6. Сравнение перспективных технологий
| Технология | Главное преимущество | Основная проблема | Статус развития | Потенциальные применения |
|---|---|---|---|---|
| Solid‑State | Высокая безопасность и энергоёмкость | Сложное производство | Пилотное производство | EV, авиация, премиальная электроника |
| Silicon Anodes | Увеличение ёмкости | Расширение и деградация | Частичное коммерческое использование | Смартфоны, EV |
| Sodium‑Ion | Низкая стоимость | Меньшая плотность энергии | Начальная коммерциализация | ESS, бюджетный транспорт |
| LFP нового поколения | Безопасность и долговечность | Ниже энергоёмкость | Массовое производство | EV, солнечные системы |
| 4680 Cells | Снижение стоимости батарей | Сложное теплоотведение | Активное масштабирование | Электромобили |
Куда движется индустрия аккумуляторов
В ближайшие годы развитие Li‑ion технологий будет направлено не только на увеличение ёмкости, но и на:
- снижение стоимости батарей,
- повышение безопасности,
- ускорение зарядки,
- снижение использования дефицитных материалов,
- упрощение переработки и повторного использования.
Именно поэтому будущее батарейной отрасли будет определяться не одной «революционной» батареей, а сочетанием различных химий и технологий для конкретных областей применения — от смартфонов и электромобилей до промышленных систем накопления энергии и авиации.
FAQ: распространённые вопросы о литий‑ионных аккумуляторах
1. Что такое литий‑ионный аккумулятор?
Литий‑ионный аккумулятор (Li‑ion) — это перезаряжаемый электрохимический элемент, в котором ионы лития перемещаются между анодом и катодом во время зарядки и разрядки. Такие батареи используются в смартфонах, ноутбуках, электромобилях и системах накопления энергии.
2. Как работает литий‑ионный аккумулятор?
При разряде ионы лития движутся от анода к катоду через электролит, а электроны проходят через внешнюю электрическую цепь, питая устройство. При зарядке процесс идёт в обратном направлении.
3. Почему литий‑ионные аккумуляторы такие энергоёмкие?
Li‑ion аккумуляторы обладают высокой плотностью энергии благодаря высокому напряжению элемента (≈3,6–3,7 В) и способности лития эффективно накапливать энергию при малой массе.
4. Почему литий‑ионные батареи могут взрываться?
Причиной является тепловой разгон — неконтролируемый рост температуры из‑за короткого замыкания, механического повреждения, перезаряда или перегрева. В критических случаях это может привести к возгоранию или выбросу горячих газов.
5. Что такое дендриты в литиевых батареях?
Дендриты — это тонкие металлические «усы» лития, которые могут образовываться при зарядке. Они способны прорасти через сепаратор и вызвать внутреннее короткое замыкание.
6. Почему не рекомендуется заряжать Li‑ion аккумулятор на морозе?
При температурах ниже 0°C возрастает риск литиевого плакирования — осаждения металлического лития на аноде. Это ускоряет деградацию батареи и повышает риск повреждения элемента.
7. Что такое BMS в литий‑ионных батареях?
BMS (Battery Management System) — это система управления аккумулятором, которая контролирует напряжение, температуру, ток и защищает батарею от перезаряда, глубокого разряда и перегрева.
8. Сколько служит литий‑ионный аккумулятор?
Типичный Li‑ion аккумулятор выдерживает приблизительно 500–1500 циклов зарядки в зависимости от химии, температуры эксплуатации, глубины разряда и режима зарядки.
9. Почему деградируют литий‑ионные аккумуляторы?
Основными причинами деградации являются высокая температура, длительное хранение при 100% заряде, быстрая зарядка, глубокие разряды и химическое старение электродов.
10. Что лучше: Li‑ion или LiFePO4?
Li‑ion аккумуляторы обладают более высокой плотностью энергии и меньшей массой, тогда как LiFePO4 обеспечивают повышенную безопасность, более длительный ресурс и лучшую термостабильность.
11. Почему формат 18650 стал таким популярным?
Формат 18650 объединил высокую энергоёмкость, стандартизированные размеры, хорошую надёжность и относительно низкую стоимость производства, что сделало его популярным в ноутбуках, электротранспорте и промышленных системах.
12. Как продлить срок службы Li‑ion аккумулятора?
Для увеличения ресурса рекомендуется избегать перегрева, не оставлять батарею надолго полностью заряженной, поддерживать уровень заряда примерно в диапазоне 20–80% и не заряжать аккумулятор при сильном морозе.
Почему деградируют литий‑ионные аккумуляторы
Несмотря на высокую энергоёмкость и эффективность, Li‑ion аккумуляторы постепенно теряют ёмкость даже при правильной эксплуатации. Этот процесс называется деградацией батареи и является результатом сложных электрохимических и механических изменений внутри элемента.
Деградация делится на два основных типа:
- Календарное старение — постепенное ухудшение характеристик со временем, даже без активного использования.
- Циклическое старение — износ батареи вследствие зарядки и разрядки.
SEI‑слой: защита и проблема одновременно
На поверхности графитового анода формируется так называемый SEI‑слой (Solid Electrolyte Interphase) — тонкая плёнка продуктов реакции электролита с анодом. Он необходим для стабильной работы батареи, поскольку:
- предотвращает дальнейшее разрушение электролита,
- пропускает ионы лития,
- блокирует электроны.
Однако с течением времени SEI‑слой утолщается, потребляя активный литий и увеличивая внутреннее сопротивление элемента. Это приводит к:
- потере ёмкости,
- снижению мощности,
- перегреву под нагрузкой.
Таблица 6. Что больше всего вредит Li‑ion батареям
| Фактор | Влияние на деградацию | Последствия |
|---|---|---|
| Высокая температура | Ускоряет химические реакции | Быстрая потеря ёмкости |
| Постоянный заряд 100% | Усиливает окисление катода | Календарное старение |
| Глубокие разряды | Стресс для электродов | Сокращение ресурса |
| Быстрая зарядка | Повышает тепловую нагрузку | Деградация анода |
| Зарядка на морозе | Риск литиевого плакирования | Повреждение элемента |
| Механические повреждения | Нарушение структуры электродов | Короткое замыкание |
Современные системы BMS частично компенсируют эти проблемы, однако полностью остановить старение литий‑ионных аккумуляторов пока невозможно.
Как продлить срок службы Li‑ion аккумулятора
Срок службы литий‑ионного аккумулятора в значительной степени зависит от режима эксплуатации. Даже небольшие изменения в привычках зарядки могут существенно повлиять на ресурс батареи.
Практические рекомендации
- Избегайте длительного нахождения батареи на 100% заряда, особенно при высокой температуре.
- Для повседневного использования оптимальным считается диапазон 20–80% SoC.
- Не допускайте сильного перегрева смартфона, ноутбука или электромобиля.
- Не заряжайте Li‑ion аккумулятор при температуре ниже 0°C.
- Избегайте глубоких разрядов до полного выключения устройства.
- Для длительного хранения рекомендуется оставлять батарею приблизительно на 40–60% заряда.
Таблица 7. Оптимальные условия эксплуатации Li‑ion батарей
| Параметр | Рекомендуемое значение |
|---|---|
| Рабочая температура | ≈15–35°C |
| Оптимальный уровень заряда | 20–80% |
| Хранение | 40–60% SoC |
| Температура хранения | ≈10–20°C |
| Быстрая зарядка | Только при умеренной температуре |
Соблюдение этих рекомендаций позволяет значительно замедлить деградацию и продлить ресурс Li‑ion аккумулятора на сотни циклов.
Безопасность литий‑ионных аккумуляторов: thermal runaway, BMS и современный защитный комплекс
Высокая плотность энергии Li‑ion аккумуляторов одновременно является главным преимуществом и источником повышенных требований к безопасности. Именно поэтому современные батареи оснащают сложными системами защиты от перегрева, короткого замыкания и перегрузок.
Что такое thermal runaway
Thermal runaway («thermal runaway», тепловой разгон) — это неконтролируемый процесс саморазгоняющегося нагрева элемента.
Он может быть вызван:
- внутренним коротким замыканием,
- механическим повреждением батареи,
- перезарядкой,
- внешним перегревом,
- дефектами производства.
При тепловом разгоне температура элемента может превышать сотни градусов Цельсия, что способно привести к возгоранию электролита или выбросу горячих газов.
Таблица 8. Какие системы защиты используются в Li‑ion батареях
| Система защиты | Назначение |
|---|---|
| BMS (Battery Management System) | Контроль напряжения, температуры и тока |
| CID (Current Interrupt Device) | Разрыв цепи при избыточном давлении |
| PTC (Positive Temperature Coefficient) | Ограничение тока при перегреве |
| Shutdown Separator | Блокировка переноса ионов при перегреве |
| Термодатчики | Мониторинг температуры элементов |
| Плавкие предохранители | Защита от короткого замыкания |
Почему безопасность стала ключевым направлением развития батарей
С ростом ёмкости аккумуляторов и распространением электромобилей требования к безопасности стали критически важными. Современные производители стремятся:
- снизить риск thermal runaway,
- повысить термостабильность катодов,
- использовать негорючие или твёрдотельные электролиты,
- улучшить алгоритмы BMS и систем охлаждения.
Именно безопасность сегодня является одним из главных факторов конкуренции между различными батарейными химиями и производителями аккумуляторных систем.
Источники и литература
- M. Stanley Whittingham. History, Evolution, and Future Status of Energy Storage. Proceedings of the IEEE, Vol. 100, Special Centennial Issue, 2012.
- John B. Goodenough, Kyu-Sung Park. The Li-Ion Rechargeable Battery: A Perspective. Journal of the American Chemical Society (JACS), 2013.
- Yoshio Nishi. Lithium ion secondary batteries; past 10 years and the future. Journal of Power Sources, 2001.
- M. Armand, J.-M. Tarascon. Building better batteries. Nature, Vol. 451, 2008.
- J.-M. Tarascon, M. Armand. Issues and challenges facing rechargeable lithium batteries. Nature, Vol. 414, 2001.
- Battery University. BU-204: How do Lithium Batteries Work?
- Battery University. BU-205: Types of Lithium-ion Batteries.
- Battery University. BU-808: How to Prolong Lithium-based Batteries.
- Sony Corporation. History of Sony Lithium-ion Battery Commercialization.
- Nobel Prize Organization. The Nobel Prize in Chemistry 2019 — Lithium-ion batteries.
- Jeff Dahn et al. Mechanisms of Lithium-Ion Battery Degradation and Aging. Dalhousie University Battery Research Publications.
- U.S. Department of Energy (DOE). Lithium-Ion Battery Basics and Safety Guidelines.
- Tesla Battery Day Technical Presentations, 2020.
- CATL Research Publications on Sodium-Ion Batteries and Advanced Cell Chemistry.
- Nitta, Wu, Lee, Yushin. Li-ion battery materials: present and future. Materials Today, 2015.
- Xu, K. Electrolytes and Interphases in Li-Ion Batteries and Beyond. Chemical Reviews, 2014.
- Goodenough, Kim. Challenges for Rechargeable Li Batteries. Chemistry of Materials, 2010.
- Scrosati, Garche. Lithium batteries: Status, prospects and future. Journal of Power Sources, 2010.


