Як працюють літій-іонні акумулятори: принцип роботи, історія, аноди, катоди та майбутнє Li-ion

Літій-іонний акумулятор (Li-ion) — це перезаряджуваний електрохімічний елемент, у якому іони літію переміщуються між анодом і катодом під час заряджання та розряджання. Завдяки високій щільності енергії Li-ion акумулятори стали основою сучасної портативної електроніки, електромобілів та систем накопичення енергії, але їхня історія починається з невдалих експериментів із металевим літієм і драматичних відгуків батарей у 1991 році.
Витоки літієвих батарей: від металевого літію до літій-іонної епохи
Піонерська робота над літієвими батареями почалася ще у 1912 році під керівництвом американського хіміка Гілберта Ньютона Льюїса (G. N. Lewis), але до реальних продуктів було далеко. Лише на початку 1970‑х років з’явилися перші комерційні неперезаряджувані (primary) літієві елементи, що використовували металевий літій як анод. Спроби створити перезаряджувані літієві акумулятори в 1980‑х роках закінчилися провалом: виявилося, що металевий літій як анод є надто нестабільним під час циклів заряд–розряд.
Важливо розрізняти два класи систем:
- Метало-літієві батареї — використовують металевий літій як анод.
- Літій-іонні батареї — застосовують графіт (або інший вуглецевий / інтеркаляційний матеріал) як анод і різні активні матеріали (оксиди металів) у катоді.
Літій — найлегший метал із максимально високим електрохімічним потенціалом, тому теоретично забезпечує найвищу питому енергію серед металевих анодних систем. Акумулятори з металевим літієм на аноді дійсно демонстрували надзвичайно високу щільність енергії, але водночас виявили серйозну проблему безпеки.
Дендрити, тепловий розгін і знаменитий відгук 1991 року
У середині 1980‑х років дослідники виявили, що при циклічному заряджанні–розряджанні на поверхні металевого літію утворюються дендрити — тонкі металеві «голки» та відгалуження. Ці дендрити проростають крізь пори сепаратора й можуть дістатися протилежного електрода, спричиняючи внутрішнє коротке замикання.
Коли це стається, опір елемента різко падає, струм зростає, і температура осередку стрімко піднімається, наближаючись до точки плавлення літію. Такий тепловий розгін може закінчитися тепловим вибухом та «викидом полум’я» — раптовим розрядом з викидом гарячих газів і полум’я. Ситуація стала настільки серйозною, що на початку 1990‑х велика кількість перезаряджуваних метало-літієвих батарей, відправлених до Японії, була відкликана після інциденту, коли акумулятор мобільного телефону викинув палаючі гази й спричинив опіки обличчя користувача.
Властива металевому літію нестабільність, особливо під час заряджання, змусила галузь практично відмовитися від металевого літію як анодного матеріалу й перейти до концепції літій-іонних систем, де літій присутній у вигляді іонів, а не «чистого» металу.
Комерціалізація літій-іонних акумуляторів: Sony, Goodenough і суперечки за патенти
У 1991 році Sony комерціалізувала перший літій-іонний акумулятор і встановила новий стандарт для портативної енергетики. Хоча енергоємність Li‑ion була нижчою, ніж у теоретичних літій-металевих систем, нова хімія виявилася суттєво безпечнішою за дотримання обмежень по напрузі й струму.
Одним із ключових фігур у розвитку Li‑ion став Джон Б. Гуденаф (John B. Goodenough, 1922–2023), який наприкінці 1970‑х років у Оксфордському університеті продемонстрував, що оксид літію‑кобальту (LiCoO₂) може слугувати високовольтним катодним матеріалом для перезаряджуваних літій‑іонних батарей. На базі цієї катодної хімії японський хімік Акіра Йошіно в компанії Asahi Kasei у 1980‑х роках створив першу комерційно придатну літій‑іонну батарею, адаптувавши розробки Гуденафа до промислового застосування в Японії. У 1991 році Sony оголосила про міжнародний патент на катод LiCoO₂, що спричинило багаторічні судові тяжби. Зрештою Sony зберегла контроль над патентом, а Гуденаф не отримав фінансової винагороди, пропорційної масштабам впливу його ідеї.
Лише пізніше, як визнання фундаментального внеску в розвиток літій-іонних технологій, Національна інженерна академія США у 2014 році присудила Гуденафу та іншим ключовим розробникам премію Чарльза Старка Дрейпера. У 2015 році Ізраїль відзначив його роботу премією у розмірі 1 млн доларів, яку Гуденаф передав Техаському інституту матеріалів для подальших досліджень у галузі матеріалознавства.
Чому літій-іонні акумулятори такі енергоємні
Головний фактор високої питомої енергії Li‑ion — висока напруга осередку близько 3,6В. У поєднанні з доволі високою ємністю це забезпечує значну енергію на одиницю маси та об’єму. Подальше вдосконалення активних матеріалів катода й анода, а також електролітів, потенційно дозволяє ще підняти щільність енергії.
Крива розряду літій-іонного елемента має відносно плоский профіль у робочому діапазоні напруги приблизно 3,7–2,8В на осередок. Це означає, що більша частина накопиченої енергії доступна в досить вузькому інтервалі напруг, що спрощує проектування електроніки живлення й підвищує ефективність використання енергії.
Таблиця 1. Порівняння основних хімій літій-іонних акумуляторів
| Хімія | Повна назва | Номінальна напруга | Щільність енергії | Безпека | Ресурс циклів | Основні переваги | Основі недоліки | Типові застосування |
|---|---|---|---|---|---|---|---|---|
| LiCoO₂ (LCO) | Літій-кобальт-оксид | 3,6–3,7 В | Дуже висока | Середня | 500–1000 | Висока енергоємність | Низька термостабільність, дорогий кобальт | Смартфони, ноутбуки, фотоапарати |
| NMC | Нікель-марганець-кобальт | 3,6–3,7 В | Висока | Середня | 1000–2000 | Баланс між ємністю, потужністю та ресурсом | Складне охолодження при високих навантаженнях | Електромобілі, системи зберігання енергії |
| NCA | Нікель-кобальт-алюміній | 3,6–3,7 В | Дуже висока | Середня-низька | 1000–1500 | Максимальна енергоємність | Вища чутливість до перегріву | Електромобілі Tesla, авіація |
| LFP | Літій-залізо-фосфат | 3,2–3,3 В | Середня | Дуже висока | 2000–7000 | Безпека, довговічність, стабільність | Нижча щільність енергії | Сонячні станції, електробуси, UPS |
| LTO | Літій-титанат | 2,3–2,4 В | Низька | Надзвичайно висока | 10000–25000 | Екстремальний ресурс і швидка зарядка | Висока ціна та низька енергоємність | Промисловість, транспорт, військові системи |
Еволюція формату 18650: від 1100 до 3000+ мА·год
Циліндричний формат 18650 (діаметр 18 мм, довжина 65 мм) став одним із найважливіших «будівельних блоків» літій-іонної енергетики.
- У 1994 році виробнича собівартість одного Li‑ion 18650 перевищувала 10 доларів США, а ємність становила близько 1100 мА·год.
- До 2001 року ціна впала нижче 3 доларів США, тоді як ємність зросла до ≈1900 мА·год.
- Сьогодні високоенергетичні 18650 перевищують 3000 мА·год, а вартість продовжує знижуватися завдяки масовому виробництву, оптимізації матеріалів та вдосконаленню процесів.
Зниження вартості, збільшення питомої енергії та відсутність високотоксичних компонентів зробили літій-іонні акумулятори універсальним рішенням для портативної електроніки, промислових систем, електричних силових агрегатів та навіть супутників.
Таблиця 2. Еволюція формату 18650
| Рік | Типова ємність | Орієнтовна ціна | Ключові особливості |
|---|---|---|---|
| 1994 | ≈1100 мА·год | >10 USD | Початок масового розвитку Li-ion |
| 2001 | ≈1900 мА·год | <3 USD | Активне здешевлення виробництва |
| 2010 | 2400–2800 мА·год | ≈2–4 USD | Широке використання в ноутбуках та EV |
| 2025+ | 3000–4000+ мА·год | Продовжує знижуватися | Кремнієві домішки та оптимізація матеріалів |
Переваги літій-іонних акумуляторів: чому вони стали стандартом
Літій-іонні батареї практично не потребують обслуговування, що різко відрізняє їх від нікелевих і свинцевих систем. Вони не мають вираженого ефекту пам’яті й не вимагають спеціальних «розрядних тренувань» для підтримання ємності. Рівень саморозряду — менше половини, ніж у NiCd і NiMH, що робить показники рівня заряду (SoC‑індикатори) набагато надійнішими.
Номінальна напруга одного осередку (≈3,6В) дозволяє безпосередньо живити мобільні телефони, планшети, цифрові фотоапарати й інші пристрої без необхідності складних багатоосередкових конфігурацій. Це спрощує шаси, зменшує вагу, знижує вартість та підвищує загальну ефективність.
Основні переваги Li‑ion:
- Висока питома енергія (Вт·год/кг) і можливість реалізації елементів із високою питомою потужністю (power cells).
- Відносно довгий циклоресурс та тривалий календарний термін служби.
- Висока ємність, низький внутрішній опір, високий кулонівський ККД.
- Простий алгоритм заряджання (постійний струм → постійна напруга) і відносно короткий час зарядки.
- Низький саморозряд (менше половини NiCd/NiMH).
Обмеження:
- Необхідність захисних схем (BMS) для запобігання перенапрузі, глибокому розряду та перегріву, що може призвести до теплового розгону.
- Деградація при високих температурах і тривалому зберіганні за високої напруги (поблизу повного заряду).
- Небажано швидко заряджати при температурах нижче 0°C (ризик літієвого плакування).
- Потреба в дотриманні транспортних правил при перевезенні великих партій Li‑ion.
Як працює літій-іонний акумулятор: анод, катод та рух іонів
Літій-іонний елемент складається з трьох ключових компонентів:
- Катод (позитивний електрод) — оксид металу (наприклад, LiCoO₂, NMC, NCA тощо), нанесений на алюмінієвий струмозбірник.
- Анод (негативний електрод) — зазвичай графіт або інший вуглецевий матеріал, нанесений на мідний струмозбірник.
- Електроліт і сепаратор — органічний рідкий електроліт із солями літію та пористий сепаратор, який пропускає іони, але блокує електрони.
Під час розряду іони літію рухаються від анода до катода через електроліт, а електрони — через зовнішнє коло, виконуючи роботу. Анод при цьому зазнає окиснення (віддає електрони), катод — відновлення (приймає електрони). Під час заряджання процес йде у зворотному напрямку: іони літію «закачуються» назад в анод, а електрони повертаються через зарядний ланцюг.
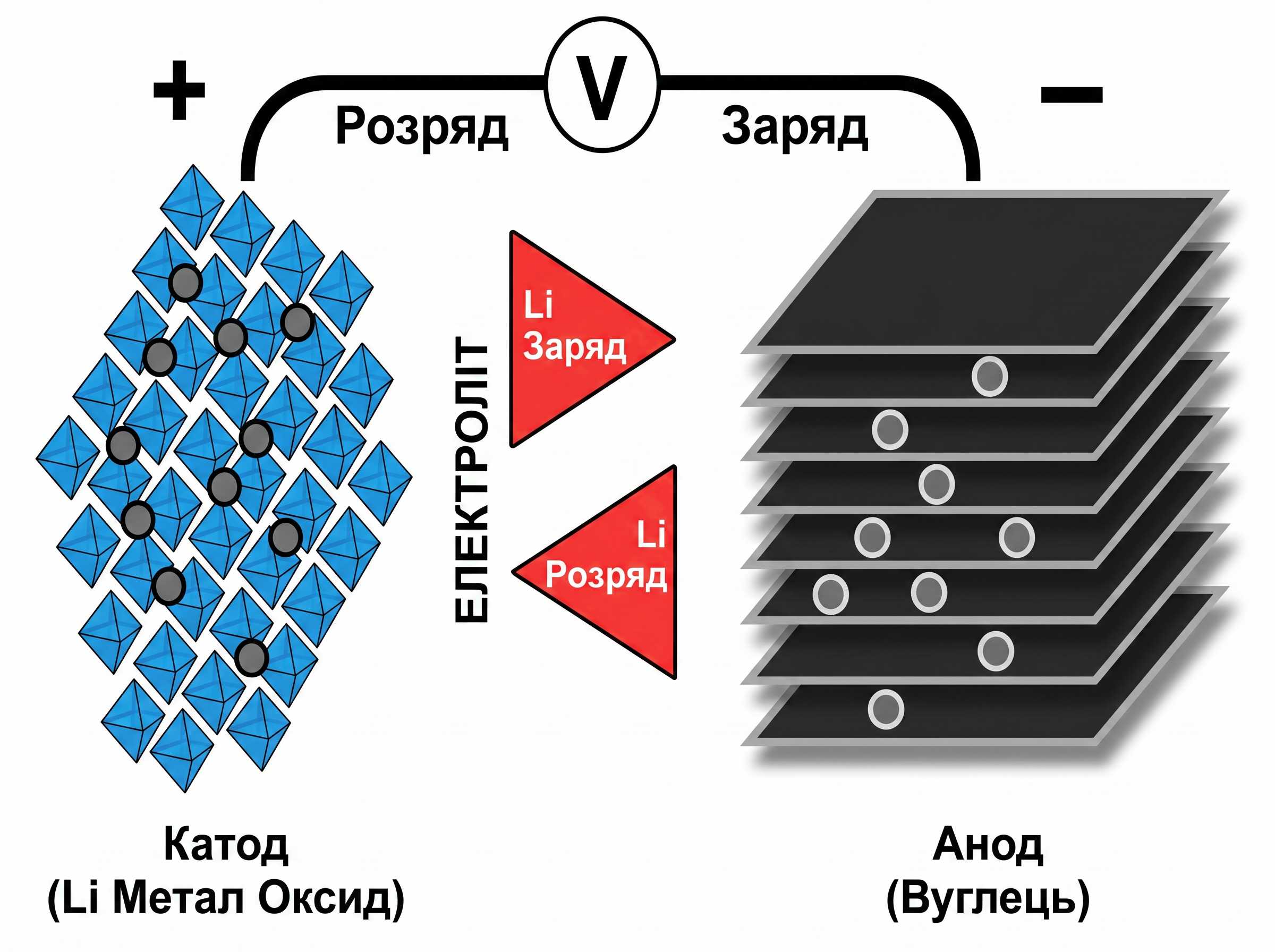
Рисунок 1: Потік іонів у літій-іонному акумуляторі.
Під час заряджання та розряджання елемента іони переміщуються між катодом (позитивний електрод) та анодом (негативний електрод). Під час розряду анод зазнає окислення або втрати електронів, а катод зазнає відновлення або посилення електронів. Заряд здійснює зворотний рух.
Від коксу до графіту та далі: еволюція анодних матеріалів
Перші літій-іонні елементи Sony використовували кокс (побічний продукт нафтохімії) як анодний матеріал. У 1997 році більшість виробників, включно із Sony, перейшли на графіт, щоб отримати більш пласку криву розряду й кращу циклічну стабільність. Графіт — це поширена форма вуглецю (знайома нам, зокрема, по грифелях олівців), яка добре інтерклюдує іони літію й має довгий термін служби.
Серед вуглецевих матеріалів для анода розрізняють:
- графіт (домінуючий на ринку)
- твердий і м’який вуглець
- нанотрубчасті форми (поки що без широкого комерційного застосування через схильність до агрегації).
У перспективі важливу роль може відіграти графен та композити на його основі, які обіцяють вищу провідність і потенційно кращі механічні властивості анода.
На рисунках типу «кривих розряду» добре видно, що сучасний графітовий анод формує набагато більш плоский профіль напруги, ніж ранні коксові варіанти, що покращує стабільність живлення навантаження.
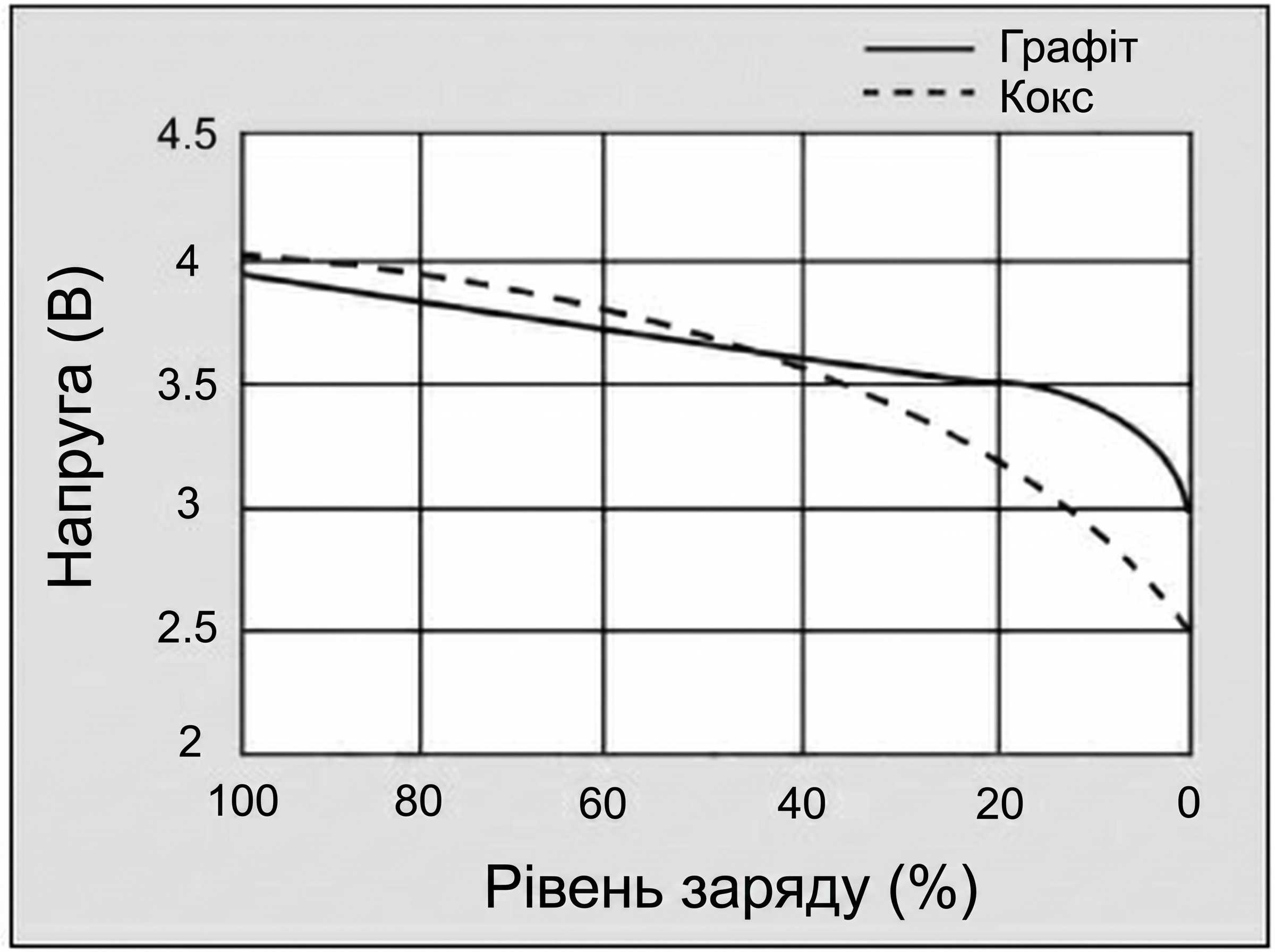
Рисунок 2: Крива розряду літій-іонного акумулятора.
Акумулятор повинен мати плоску криву напруги в робочому діапазоні розряду. Сучасний графітовий анод робить це краще, ніж ранній коксовий варіант. Надано Cadex.
Кремнієві та титантові аноди: 10× потенціал і проблеми розширення
Щоб збільшити енергоємність Li‑ion, виробники експериментують із додаванням кремнію до анода. На атомному рівні співвідношення вуглець : літій складає приблизно 6:1 — шість атомів вуглецю можуть зв’язати один іон літію. Кремній же здатен зв’язувати до чотирьох іонів літію на один атом, що теоретично відкриває можливість збільшити ємність анода в ≈10 разів у порівнянні з чистим графітом.
Головна проблема — об’ємне розширення: під час заряджання кремнієвий анод може збільшуватися в об’ємі до 300%, що призводить до механічних руйнувань, тріщин та швидкої деградації. Тому чисто кремнієві аноди на нинішньому етапі непрактичні; натомість виробники додають невеликі кількості кремнію (3–5%) у графітову матрицю, підвищуючи ємність без катастрофічної втрати ресурсу.
Інший цікавий напрям — використання наноструктурованого літій-титанату (LTO) як анодного матеріалу. LTO забезпечує:
- дуже довгий циклоресурс (десятки тисяч циклів)
- високі навантажувальні можливості
- відмінні низькотемпературні характеристики
- підвищену безпеку та термостабільність, але за рахунок нижчої питомої енергії й більшої вартості.
Таблиця 3. Порівняння анодних матеріалів у Li-ion акумуляторах
| Матеріал анода | Питома ємність | Переваги | Недоліки | Стан використання |
|---|---|---|---|---|
| Графіт | ≈372 мА·год/г | Стабільність, низька ціна, довгий ресурс | Обмежена ємність | Домінує на ринку |
| Кремній | До ≈4200 мА·год/г | Дуже висока теоретична ємність | Розширення до 300%, деградація | Використовується у композитах |
| LTO | ≈175 мА·год/г | Безпека, ресурс, швидка зарядка | Низька енергоємність | Спеціалізовані системи |
| Твердий вуглець | Середня | Стабільність і низька вартість | Нижча провідність | Частково використовується |
| Графенові композити | Потенційно дуже висока | Висока провідність і механічна міцність | Висока ціна та складне виробництво | Експериментальні технології |
«Енергетичні», «силові» та гібридні елементи Li‑ion
Модифікуючи матеріали анода й катода, виробники можуть настроювати елементи під різні задачі:
- Енергетичний елемент (energy cell) — максимізує питому енергію, забезпечуючи тривалий час роботи, але має нижчу питому потужність.
- Силовий елемент (power cell) — оптимізований під високі струми й пікові навантаження, жертвуючи частиною ємності.
- Гібридний елемент (hybrid cell) — компромісний варіант, який пропонує баланс між енергоємністю й потужністю.
Ще одна вісь налаштування — співвідношення кобальту й нікелю в катоді:
- збільшення частки нікелю зменшує собівартість і підвищує ємність,
- але знижує термостабільність і безпеку.
Початківці намагаються швидко вийти на ринок, пропонуючи високі енергоємності й низькі ціни, але це часто відбувається за рахунок довговічності й безпеки. Добросовісні виробники приділяють пріоритетну увагу саме безпеці, стабільності та прогнозованому старінню.
Таблиця 4. Порівняння типів Li-ion елементів за призначенням
| Тип елемента | Основний пріоритет | Питома енергія | Питома потужність | Типові застосування |
|---|---|---|---|---|
| Energy Cell | Максимальна ємність | Дуже висока | Середня | Ноутбуки, смартфони, електромобілі |
| Power Cell | Високий струм | Середня | Дуже висока | Електроінструмент, дрони, спорткари |
| Hybrid Cell | Баланс параметрів | Висока | Висока | Універсальні батарейні системи |
Структура осередку Li‑ion і коротке резюме плюсів/мінусів
Типовий літій-іонний осередок має таку будову:
- Катод: шар оксиду металу на алюмінієвому колекторі.
- Анод: шар графіту / вуглецю на мідному колекторі.
- Сепаратор: пориста полімерна плівка, що розділяє електроди й пропускає тільки іони.
- Електроліт: органічний розчинник із літієвою сіллю, який переносить іони між електродами.
Узагальнені переваги Li‑ion:
- Висока питома енергія та можливість реалізувати високі навантаження у «силових» варіантах.
- Довгий циклоресурс і тривалий термін зберігання.
- Низький внутрішній опір, високий ККД, простий зарядний алгоритм.
- Низький саморозряд і відсутність вираженого ефекту пам’яті.
Узагальнені обмеження:
- Потреба в BMS і захисних схемах для уникнення теплового розгону.
- Чутливість до високої температури й тривалого перебування на високій напрузі (повному заряді).
- Обмеження на швидку зарядку при низьких температурах.
- Транспортні вимоги при перевезенні великих партій акумуляторів.
Літій-іонні акумулятори, попри свої обмеження, стали ключовою технологією енергетичного переходу — від смартфонів і ноутбуків до електромобілів і систем накопичення енергії, задаючи напрям розвитку матеріалознавства, електрохімії та інженерії батарей на десятиліття вперед
Таблиця 5. Порівняння Li-ion, NiMH та свинцево-кислотних акумуляторів
| Параметр | Li-ion | NiMH | Свинцево-кислотний |
|---|---|---|---|
| Щільність енергії | Висока | Середня | Низька |
| Саморозряд | Низький | Високий | Низький |
| Ефект пам’яті | Практично відсутній | Помірний | Відсутній |
| Маса | Низька | Середня | Висока |
| Ресурс циклів | 500–3000+ | 300–700 | 200–500 |
| Обслуговування | Мінімальне | Мінімальне | Може потребувати обслуговування |
| Типові застосування | Електроніка, EV, ESS | Побутова техніка | UPS, автостартери |
Майбутнє літій-іонних акумуляторів: сучасні тренди та нові технології
Попри домінування класичних Li-ion акумуляторів, галузь батарейних технологій переживає один із найшвидших етапів розвитку в історії електрохімії. Виробники електромобілів, портативної електроніки та систем накопичення енергії активно працюють над збільшенням щільності енергії, швидкості заряджання, ресурсу та безпеки акумуляторів.
Серед ключових напрямів розвитку — твердотільні батареї (solid-state batteries), кремнієві аноди, натрій-іонні системи, високонікелеві катоди та нові виробничі технології на кшталт dry electrode manufacturing.
Твердотільні акумулятори (Solid-State Batteries)
Твердотільні акумулятори замінюють рідкий органічний електроліт твердим іонопровідним матеріалом. Це потенційно дозволяє:
- значно підвищити безпеку,
- зменшити ризик теплового розгону,
- використовувати металевий літій як анод,
- підвищити щільність енергії на 30–70%.
Головними проблемами solid-state залишаються висока вартість, складність виробництва та деградація контактів між твердими матеріалами під час циклів заряджання.
Кремнієві аноди нового покоління
Одним із найактивніших напрямів розвитку є поступове збільшення частки кремнію в анодах. Кремній має теоретичну ємність у багато разів вищу за графіт, що дозволяє:
- збільшити автономність електромобілів,
- зменшити масу батарей,
- підвищити швидкість заряджання.
Сучасні виробники вже застосовують графіт-кремнієві композити, але високий рівень об’ємного розширення кремнію все ще залишається ключовою інженерною проблемою.
Натрій-іонні акумулятори (Sodium-Ion)
Натрій-іонні батареї (Na-ion) вважаються перспективною альтернативою Li-ion для стаціонарних систем накопичення енергії та бюджетного транспорту.
Їхні головні переваги:
- нижча вартість сировини,
- менша залежність від літію та кобальту,
- краща робота при низьких температурах.
Недоліком натрій-іонних систем поки що є нижча щільність енергії порівняно з класичними Li-ion акумуляторами.
Високонікелеві катоди та зменшення частки кобальту
Сучасні катодні матеріали поступово переходять до високонікелевих композицій (NMC 811, NCA тощо), які дозволяють збільшити енергоємність і знизити використання дорогого кобальту.
Однак збільшення частки нікелю одночасно:
- підвищує чутливість до перегріву,
- ускладнює термостабілізацію,
- підвищує вимоги до систем охолодження та BMS.
Технологія dry electrode manufacturing
Одним із найперспективніших напрямів виробництва батарей є dry electrode manufacturing — технологія нанесення електродів без використання рідких розчинників.
Переваги такого підходу:
- зменшення енергоспоживання виробництва,
- спрощення технологічного процесу,
- зниження собівартості батарей,
- менший екологічний вплив.
Ця технологія активно досліджується для майбутніх високоефективних акумуляторних платформ.
Формат 4680 та нове покоління циліндричних осередків
Нові циліндричні елементи формату 4680 (46 × 80 мм) створюються для збільшення енергоємності та зменшення вартості батарейних модулів.
Порівняно з 18650 та 21700, формат 4680 забезпечує:
- вищу енергетичну щільність,
- меншу кількість з’єднань у батарейному пакеті,
- краще співвідношення маси до ємності,
- зниження виробничих витрат.
Водночас великі осередки створюють нові виклики у сфері тепловідведення та контролю температури.
Порівняння перспективних батарейних технологій
Таблиця 6. Порівняння перспективних технологій
| Технологія | Головна перевага | Основна проблема | Стан розвитку | Потенційні застосування |
|---|---|---|---|---|
| Solid-State | Висока безпека та енергоємність | Складне виробництво | Пілотне виробництво | EV, авіація, преміальна електроніка |
| Silicon Anodes | Збільшення ємності | Розширення та деградація | Часткове комерційне використання | Смартфони, EV |
| Sodium-Ion | Низька вартість | Менша щільність енергії | Початкова комерціалізація | ESS, бюджетний транспорт |
| LFP нового покоління | Безпека та довговічність | Нижча енергоємність | Масове виробництво | EV, сонячні системи |
| 4680 Cells | Зменшення вартості батарей | Складне тепловідведення | Активне масштабування | Електромобілі |
Куди рухається індустрія акумуляторів
У найближчі роки розвиток Li-ion технологій буде спрямований не лише на збільшення ємності, але й на:
- зниження вартості батарей,
- підвищення безпеки,
- швидшу зарядку,
- зменшення використання дефіцитних матеріалів,
- спрощення переробки та повторного використання.
Саме тому майбутнє акумуляторної галузі визначатиметься не однією «революційною» батареєю, а поєднанням різних хімій та технологій для конкретних сфер застосування — від смартфонів і електромобілів до промислових систем накопичення енергії та авіації.
FAQ: поширені питання про літій-іонні акумулятори
1. Що таке літій-іонний акумулятор?
Літій-іонний акумулятор (Li-ion) — це перезаряджуваний електрохімічний елемент, у якому іони літію переміщуються між анодом і катодом під час заряджання та розряджання. Такі батареї використовуються у смартфонах, ноутбуках, електромобілях та системах накопичення енергії.
2. Як працює літій-іонний акумулятор?
Під час розряду іони літію рухаються від анода до катода через електроліт, а електрони проходять через зовнішнє електричне коло, живлячи пристрій. Під час заряджання процес відбувається у зворотному напрямку.
3. Чому літій-іонні акумулятори такі енергоємні?
Li-ion акумулятори мають високу щільність енергії завдяки високій напрузі осередку (≈3,6–3,7В) та здатності літію ефективно накопичувати енергію при малій масі.
4. Чому літій-іонні батареї можуть вибухати?
Причиною є тепловий розгін — неконтрольоване підвищення температури через коротке замикання, механічне пошкодження, перезаряд або перегрів. У критичних випадках це може призвести до займання або викиду гарячих газів.
5. Що таке дендрити у літієвих батареях?
Дендрити — це тонкі металеві відростки літію, які можуть утворюватися під час заряджання. Вони здатні проростати крізь сепаратор і викликати внутрішнє коротке замикання.
6. Чому не рекомендується заряджати Li-ion акумулятор на морозі?
При температурах нижче 0°C зростає ризик літієвого плакування — осадження металевого літію на аноді. Це прискорює деградацію батареї та підвищує ризик пошкодження осередку.
7. Що таке BMS у літій-іонних батареях?
BMS (Battery Management System) — це система керування акумулятором, яка контролює напругу, температуру, струм та захищає батарею від перезаряду, глибокого розряду і перегріву.
8. Скільки служить літій-іонний акумулятор?
Типовий Li-ion акумулятор витримує приблизно 500–1500 циклів заряджання залежно від хімії, температури експлуатації, глибини розряду та режиму заряджання.
9. Чому деградують літій-іонні акумулятори?
Основними причинами деградації є висока температура, тривале зберігання при 100% заряді, швидке заряджання, глибокі розряди та хімічне старіння електродів.
10. Що краще: Li-ion чи LiFePO4?
Li-ion акумулятори мають вищу щільність енергії та меншу вагу, тоді як LiFePO4 забезпечують більшу безпеку, довший ресурс і кращу термостабільність.
11. Чому формат 18650 став таким популярним?
Формат 18650 поєднав високу енергоємність, стандартизовані розміри, хорошу надійність та відносно низьку вартість виробництва, що зробило його популярним у ноутбуках, електротранспорті та промислових системах.
12. Як продовжити термін служби Li-ion акумулятора?
Для збільшення ресурсу рекомендується уникати перегріву, не залишати батарею надовго повністю зарядженою, підтримувати рівень заряду приблизно в межах 20–80% та не заряджати акумулятор при сильному морозі.
Чому деградують літій-іонні акумулятори
Попри високу енергоємність і ефективність, Li-ion акумулятори поступово втрачають ємність навіть за правильної експлуатації. Цей процес називається деградацією батареї й є результатом складних електрохімічних та механічних змін усередині осередку.
Деградація поділяється на два основні типи:
- Календарне старіння — поступове погіршення характеристик з часом, навіть без активного використання.
- Циклічне старіння — зношування батареї внаслідок заряджання та розряджання.
SEI-шар: захист і проблема одночасно
На поверхні графітового анода формується так званий SEI-шар (Solid Electrolyte Interphase) — тонка плівка продуктів реакції електроліту з анодом. Вона необхідна для стабільної роботи батареї, оскільки:
- запобігає подальшому руйнуванню електроліту,
- пропускає іони літію,
- блокує електрони.
Однак із часом SEI-шар потовщується, споживаючи активний літій та збільшуючи внутрішній опір осередку. Це призводить до:
- втрати ємності,
- зниження потужності,
- перегріву під навантаженням.
Таблиця 6. Що найбільше шкодить Li-ion батареям
| Фактор | Вплив на деградацію | Наслідки |
|---|---|---|
| Висока температура | Прискорює хімічні реакції | Швидка втрата ємності |
| Постійний заряд 100% | Підвищує окиснення катода | Календарне старіння |
| Глибокі розряди | Стрес для електродів | Скорочення ресурсу |
| Швидка зарядка | Підвищує теплове навантаження | Деградація анода |
| Зарядка на морозі | Ризик літієвого плакування | Пошкодження осередку |
| Механічні пошкодження | Порушення структури електродів | Коротке замикання |
Сучасні системи BMS частково компенсують ці проблеми, але повністю зупинити старіння Li-ion акумуляторів поки що неможливо.
Як продовжити термін служби Li-ion акумулятора
Термін служби літій-іонного акумулятора значною мірою залежить від режиму експлуатації. Навіть невеликі зміни у звичках заряджання можуть суттєво вплинути на ресурс батареї.
Практичні рекомендації
- Уникайте тривалого перебування батареї на 100% заряду, особливо при високій температурі.
- Для повсякденного використання оптимальним вважається діапазон 20–80% SoC.
- Не допускайте сильного перегріву смартфона, ноутбука чи електромобіля.
- Не заряджайте Li-ion акумулятор при температурі нижче 0°C.
- Уникайте глибоких розрядів до повного вимкнення пристрою.
- Для довготривалого зберігання рекомендується залишати батарею приблизно на 40–60% заряду.
Таблиця 7. Оптимальні умови експлуатації Li-ion батарей
| Параметр | Рекомендоване значення |
|---|---|
| Робоча температура | ≈15–35°C |
| Оптимальний рівень заряду | 20–80% |
| Зберігання | 40–60% SoC |
| Температура зберігання | ≈10–20°C |
| Швидка зарядка | Лише за помірної температури |
Дотримання цих рекомендацій дозволяє суттєво сповільнити деградацію та продовжити ресурс Li-ion акумулятора на сотні циклів.
Безпека літій-іонних акумуляторів: thermal runaway, BMS та сучасний захист
Висока щільність енергії Li-ion акумуляторів одночасно є і головною перевагою, і джерелом підвищених вимог до безпеки. Саме тому сучасні батареї оснащуються складними системами захисту від перегріву, короткого замикання та перевантажень.
Що таке thermal runaway
Thermal runaway («тепловий розгін») — це неконтрольований процес самоприскорюваного нагріву осередку.
Він може бути спричинений:
- внутрішнім коротким замиканням,
- механічним пошкодженням батареї,
- перезарядом,
- зовнішнім перегрівом,
- дефектами виробництва.
Під час теплового розгону температура осередку може перевищувати сотні градусів Цельсія, що здатне призвести до займання електроліту або викиду гарячих газів.
Таблиця 8. Які системи захисту використовуються в Li-ion батареях
| Система захисту | Призначення |
|---|---|
| BMS (Battery Management System) | Контроль напруги, температури та струму |
| CID (Current Interrupt Device) | Розрив кола при надлишковому тиску |
| PTC (Positive Temperature Coefficient) | Обмеження струму при перегріві |
| Shutdown Separator | Блокування переносу іонів при перегріванні |
| Термодатчики | Моніторинг температури осередків |
| Плавкі запобіжники | Захист від короткого замикання |
Чому безпека стала ключовим напрямом розвитку батарей
Із зростанням ємності акумуляторів та поширенням електромобілів вимоги до безпеки стали критично важливими. Сучасні виробники прагнуть:
- зменшити ризик thermal runaway,
- підвищити термостабільність катодів,
- використовувати негорючі або твердотільні електроліти,
- покращити алгоритми BMS та охолодження.
Саме безпека сьогодні є одним із головних факторів конкуренції між різними батарейними хіміями та виробниками акумуляторних систем.
Джерела та література
- M. Stanley Whittingham. History, Evolution, and Future Status of Energy Storage. Proceedings of the IEEE, Vol. 100, Special Centennial Issue, 2012.
- John B. Goodenough, Kyu-Sung Park. The Li-Ion Rechargeable Battery: A Perspective. Journal of the American Chemical Society (JACS), 2013.
- Yoshio Nishi. Lithium ion secondary batteries; past 10 years and the future. Journal of Power Sources, 2001.
- M. Armand, J.-M. Tarascon. Building better batteries. Nature, Vol. 451, 2008.
- J.-M. Tarascon, M. Armand. Issues and challenges facing rechargeable lithium batteries. Nature, Vol. 414, 2001.
- Battery University. BU-204: How do Lithium Batteries Work?
- Battery University. BU-205: Types of Lithium-ion Batteries.
- Battery University. BU-808: How to Prolong Lithium-based Batteries.
- Sony Corporation. History of Sony Lithium-ion Battery Commercialization.
- Nobel Prize Organization. The Nobel Prize in Chemistry 2019 — Lithium-ion batteries.
- Jeff Dahn et al. Mechanisms of Lithium-Ion Battery Degradation and Aging. Dalhousie University Battery Research Publications.
- U.S. Department of Energy (DOE). Lithium-Ion Battery Basics and Safety Guidelines.
- Tesla Battery Day Technical Presentations, 2020.
- CATL Research Publications on Sodium-Ion Batteries and Advanced Cell Chemistry.
- Nitta, Wu, Lee, Yushin. Li-ion battery materials: present and future. Materials Today, 2015.
- Xu, K. Electrolytes and Interphases in Li-Ion Batteries and Beyond. Chemical Reviews, 2014.
- Goodenough, Kim. Challenges for Rechargeable Li Batteries. Chemistry of Materials, 2010.
- Scrosati, Garche. Lithium batteries: Status, prospects and future. Journal of Power Sources, 2010.


